西宮の家庭教師ダイアログによる過去問解説。今回は西宮市にある兵庫医科大学の過去問です。
もくじ
1 浸透圧

「浸透圧」に関する問題です。(5)は計算量も多くかなりの難問です。
(1)難易度:★★☆☆☆
[実験1]における水溶液の浸透圧はピストンとおもりによって加えられた圧力に等しくなります。よって、ピストンとおもりの質量の和から圧力を計算します。
(350+30)÷10=38[g/㎤]
この圧力を単位Paで表せばいいことになります。
水銀柱760mmが1気圧1.0×10⁵Paに相当することから計算します。
水銀の密度は13.6g/㎤だから、水銀柱760mmの圧力を底面積1㎠あたりの質量としてあらわすと、76×13.6=1033.6[g/㎠]
これが1気圧1.0×10⁵Paに相当するから、
1[g/㎤]→ \frac{1.0×10⁵}{1033.6}[Pa]
と換算できるので、38g/㎤をPaであらわすと、
38× \frac{1.0×10⁵}{1033.6} =3676.47…≒3.7×10³[Pa]
(2)難易度:★★☆☆☆
イノシトールと尿素のモル濃度の和をc[mol/L]とおくと、ファントホッフの法則(π=cRT)より、
c = \frac{3.68×10³ }{8.31×10³×300} = 0.00148…(mol/L)
よって、この水溶液100mLに含まれるイノシトールと尿素の物質量の和は、
\frac{100}{1000} × 0.00148 = 0.000148=1.5×10⁻⁴[mol]
(3)難易度:★★☆☆☆
イノシトールC₆H₁₂O₆=180、尿素CH₄N₂O=60だから、イノシトールと尿素の質量をそれぞれx㎎、y㎎とおくと、
x+y=11
\frac{x÷1000}{180} + \frac{y÷1000}{60} = 0.000148
これを解いて、x=3.18、y=7.82
よって、含まれているイノシトールは3.2㎎。
(4)難易度:★★☆☆☆
XY₂の分子量はMだから、wgのXY₂の物質量は\frac{w}{M}mol。これが50mlの水溶液に溶けているから、電離前のXY₂濃度は、
\frac{w}{M} ÷ \frac{50}{1000} = \frac{20w}{M}(mol)【ア】
電離度0.4より、それぞれの物質の電離前、変化量、平衡時のモル濃度をまとめると下表のようになる。
| (mol/L) | XY₂ | → | X²⁺ | + | 2Y |
| 電離前 | \frac{20w}{M}【ア】 | 0 | 0 | ||
| 変化量 | -\frac{8w}{M} | +\frac{8w}{M} | +\frac{16w}{M} | ||
| 平衡時 | \frac{12w}{M}【イ】 | \frac{8w}{M}【ウ】 | \frac{16w}{M}【エ】 |
よって、化学種全体の濃度は \frac{12w}{M} + \frac{8w}{M} + \frac{16w}{M} = \frac{36w}{M}【オ】
この水溶液の示す浸透圧が0.20mol/LのNaCl水溶液の浸透圧と等しいから、
\frac{36w}{M} =0.20×2
よって、M=36w÷0.4=90w【カ】
(5)難易度:★★★★☆
液面がとまったときのNaCl水溶液とAg₂CrO₄水溶液のモル濃度をそれぞれa(mol/L)、b(mol/L)とおきます。
液面停止時、NaCl水溶液は100mlから120mlとなり、Ag₂CrO₄水溶液は100mlから80mlとなっているから、Na⁺、Cl⁻、Ag⁺、CrO₄²⁻のモル濃度をまとめると下表のようになります。
| (mol/L) | Na⁺ | Cl⁻ | Ag⁺ | CrO₄²⁻ |
| はじめ | \frac{6a}{5} | \frac{6a}{5} | \frac{2b}{5} | \frac{4b}{5} |
| 液面停止時 | a | a | 2b | b |
液面が止まったとき、Ag₂CrO₄が沈殿をはじめていますから、
Ksp=[Ag⁺]²[CrO₄²⁻]=(2b)²・b=4.0×10⁻¹²(mol³/L³)
これを解いて、b=1.0×10⁻⁴
また、液面が止まったとき4cmの液面差が生じています。これは、NaCl水溶液とAg₂CrO₄水溶液の浸透圧差によるものと考えられるから、ファントホッフの法則(π=cRT)より、
4× \frac{1.0×10⁵}{1033.6} ={(a+a)-(2b+b)}×8.3×10³ × 300
2a-3b=0.0001554…
b=1.0×10⁻⁴より、a=0.0002277…
よって、はじめのNaCl水溶液の濃度は、 \frac{6a}{5} =0.0002733…≒2.7×10⁻⁴(mol/L)
2 コロイド粒子と界面活性剤

「コロイド粒子と界面活性剤」に関する問題です。どちらも油断して見逃しやすい分野です。やはり教科書をすみずみまで勉強する必要があることを再確認させられますね。設問自体は基本的な知識を問うものです。
(1)難易度:★☆☆☆☆
コロイド粒子の大きさは、10⁻⁹~10⁻⁷mですので、アが正解です。

分かりやすいように単位を変えると、
(ア)10⁻⁹~10⁻⁷m は1~100nm
(イ)10⁻⁵~10⁻⁴m は0.01~0.1mm
(ウ)10⁻²~10⁻¹m は1~10cm
(ウ)はどう考えても大きすぎますね。(イ)も肉眼でギリギリ見えないくらいのレベルですが、コロイドの定義としてはやはり大きすぎます。
(2)難易度:★★★☆☆
一つ一つ確認してみましょう。
(ア)シリカゲルはケイ酸の固体の中に小さな気泡をもち(多孔質)、そこに水を吸着することで吸湿材として利用されます。つまり、分散媒が固体、分散質が気体。よって「き」です。
(イ)砂糖水は、スクロースの「水溶液」ですので、コロイドではありません。よって「け」です。
(ウ)細かい泡は、液体の中に小さな気体の集まりがありますので、分散媒が液体、分散質が気体。よって「く」です。
(エ)マシュマロは、砂糖、卵白、ゼラチン、水あめを主原料とし、多くの気泡を含んでいます。流動性がないことから、分散媒が固体、分散質が気体。よって「き」です。
(オ)煙の成分のうち、いわゆる「すす」は炭素の集まった粒子です。分散媒が気体、分散質が固体、よって「う」です。
(カ)墨汁は「にかわ」を保護コロイドとし、すす(炭素の粒)が水中に分散しています。分散媒が液体、分散質が固体。よって「い」です。
(キ)サファイアは酸化アルミニウムの結晶中に微量の酸化鉄などが分散されているとみなせます。分散媒も分散質が固体。よって「あ」です。
(ク) 豆乳は水に浸した大豆をすりつぶし、水を加えて煮た後、ろ過した液体です。豆乳において分散しているのは、タンパク質と会合した脂質です。大豆に含まれる脂質は脂肪油、つまり、常温で液体なので分散媒も分散質も液体。よって「お」です。
(ケ)ゼリーは寒天(いわゆる食物繊維)の網の目の中に水分子の集合したコロイド粒子分散していると理解できます。つまり分散媒が固体、分散質が液体。よって「え」です。
(コ)霧は細かい水の粒が空気中に分散したものです。 つまり分散媒が気体、分散質が液体。よって「か」です。

うーん。あまり良い問題ではありませんね。
「泡」と呼ばれるもののすべてがコロイドになっているとはとても言えません。
ものが燃えた時に出る「煙」のうち、白いものについては主成分はほとんど霧と同じ(水の粒)です。
言葉によっては定義があいまいで選択が難しいものもあります。もう少し説明がほしいところです。
(3)難易度:★★☆☆☆
【A】水中で1つの分子でコロイド粒子になるものを分子コロイドといいます。
【B】【C】親水基を多く持っているコロイドを親水コロイドといい、これに多量の電解質を加えると沈殿する現象を塩析といいます。
【D】【E】【F】水酸化鉄(Ⅲ)などが水中で分散してできるコロイドを分散コロイドといい、疎水コロイドに分類されます。疎水コロイドに電解質を少量加えると沈殿する現象を凝析といいます。
【G】界面活性剤は、水の表面張力を小さくします。
【H】ミセルコロイドのことを会合コロイドともいいます。
(4)難易度:★★☆☆☆
(ⅰ)本文より、界面活性剤分子は濃度が高くなると界面をおおいつくし、その後、さらに濃度が高まるとミセルを形成し始めます。グラフよりXの濃度が8.0mmol/Lまで高まると、それ以上表面張力が小さくならなくなり、ここでXが海面を覆いつくしたことが読み取れます。言い換えるとここからミセル形成が始まるということであり、臨界ミセル濃度でもあるといえます。
よって、8.0mmol/L。
(ⅱ) 水溶液中に8.0×10⁻²mol/LふくまれるXのうち、 8.0mmol/L(= 8.0×10⁻³mol/L )ぶんが界面をおおうと考えられるので、ミセルを形成するのはその残りです。よって、ミセルの濃度は、
\frac{8.0×10⁻²-8.0×10⁻³}{60}=1.2×10⁻³[mol/L]
(ⅲ)100mLに含まれるミセルの物質量は、
1.2×10⁻³ × \frac{100}{1000} = 1.2×10⁻⁴ [mol]
これを個数で表したいので、アボガドロ定数をかけて、
1.2×10⁻⁴ × 6.0×10²³=7.2×10¹⁹ [個]
(5)難易度:★★☆☆☆
ただの水に空気を吹き込んでも、球を形成する前に表面張力により割れてしまいます。界面活性剤を加えると、表面張力が小さくなって球を形成することができるようになります。
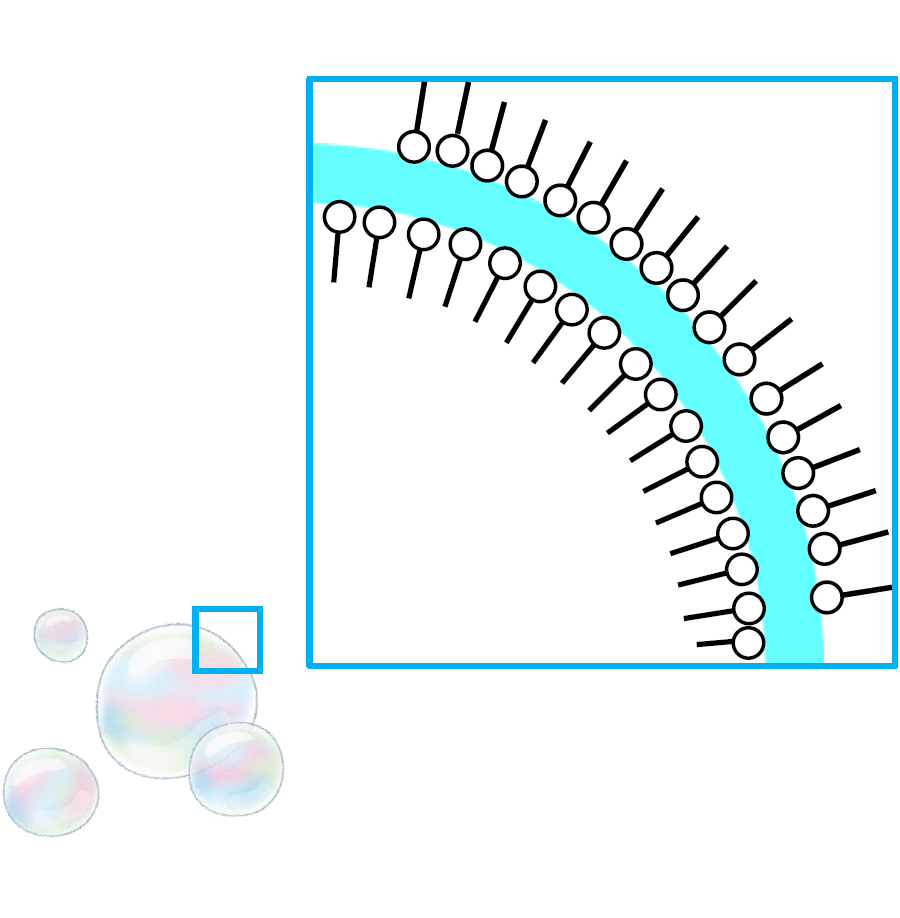
シャボン玉では、下図のように水の表面を界面活性剤分子がおおうように並ぶことになります。
モデルを描く時のポイントとしては、
・親水部を水膜側、疎水部を空気側に向け、界面に垂直に描く
・内側にも界面は存在するので内側にも並べて描く
ことに気を付ければよいでしょう。
3 不飽和結合と付加反応

「不飽和結合と付加反応」に関する問題です。標準的な難易度ですね。
(1)難易度:★★★☆☆
(ⅰ) 塩化カルシウムは水を吸収しますが、ソーダ石灰は水と二酸化炭素の両方を吸収します。よって、発生した二酸化炭素の質量のみを求めるためには、前もって水を塩化カルシウムに吸収させておく必要があります。
(ⅱ)Aの分子式をCxHxとおきます。Aを燃焼させたときの化学反応式は、
CxHx + \frac{5x}{4}O₂ → xCO₂ + \frac{x}{2}H₂O
となります。
塩化カルシウムに吸収させた水が36mg、物質量は2.0×10⁻³molなので、係数比より、発生したCO₂は4.0×10⁻³molです。
その質量は、
44×(4.0×10⁻³)=176×10⁻³[g] → 176mg
(ⅲ)反応前後で気体の体積が変わらないことから、反応前後で気体全体の物質量の和が変化しないということなので、
1+ \frac{5x}{4} =x+\frac{x}{2} これを解いて、x=4
よって、Aの分子式はC₄H₄
(ⅳ)化合物C₄H₄の構造式のうち、鎖状化合物はHC≡C-C=CH₂のみです。
(2)難易度:★★★☆☆
(ⅰ)(ア)ベンゼンの2つの水素原子を臭素原子に置換したジブロモベンゼンにはo(オルト)位、m(メタ)位、p(パラ)位の3種類の構造異性体があります。
(イ)ベンゼンの3つの水素原子を臭素原子に置換したトリブロモベンゼンには3種類の構造異性体があります。
(ウ) 化合物Bの2つの水素原子を臭素原子に置換した化合物には下図の3種類の構造異性体があります。
(エ)化合物Bの3つの水素原子を臭素原子に置換した化合物には下図の3種類の構造異性体があります。



(ⅱ)下図のように、四角形の対角線上にある2つの炭素原子に臭素原子がくっついた構造を考えます。これを鏡に映した構造は元の構造とかさねることができません。
(3)難易度:★★★☆☆
(ⅰ)化合物Cの分子式をCyHyとおきます。本文に「臭素とCが物質量比1:1で反応」とありますから、その化学反応式は、
CyHy + Br₂ → CyHyBr₂
Br₂=160であり、付加したBr₂の質量は、396-156=240[mg]だから、その物質量は、
\frac{240}{1000} ÷ 160 = 1.5×10⁻³[mol]
係数比より、反応した化合物Cの物質量も1.5×10⁻³ molであり、分子量を計算すると、
\frac{156}{1000} ÷ 1.5×10⁻³ = 104
CyHy=12y+y=13y=104 より、y=8
よって、Cの分子式は、C₈H₈
(ⅱ)通常、ベンゼン環に対して臭素の付加反応は起こりません。よって、本文の臭素の付加はベンゼン環以外の不飽和結合で起きていることが分かります。
よって、化合物Cは下図のような構造であり、これはスチレンです。
これを付加重合させると、高分子化合物であるポリスチレンになります。

(ⅲ)スチレンとブタジエンをまぜて重合させると、SBR(スチレンブタジエンゴム)が得られます。この高分子化合物のブタジエン部分には二重結合が1つ残っているため、水素分子を1つ付加させることができます。
まず、付加した水素分子の物質量は、
\frac{PV}{RT} = \frac{1.0×10⁵×298.8}{8.3×10³×300} =12[mol]
よって、960gの化合物Eの中には12molの二重結合が残っており、同物質量のブタジエン部を含むことになります。ブタジエンC₄H₆=54だから、960gの化合物Eのうち、54×12=648[g]はブタジエン由来であることが分かります。
一方残りの960ー648=312[g]はスチレン(C₈H₈=104)部であり、その物質量は312÷104=3[mol]。
よって、E中のスチレンと1,3-ブタジエンの物質量の比は、3:12=1:4
過去問はただやるだけでは何の意味もありません。以下のリンク先の「過去問演習のポイント」をご一読ください。
.png)